文章出處:公告通知 網責任編輯: 金飛鷹 閱讀量: 發表時間:2024-03-01
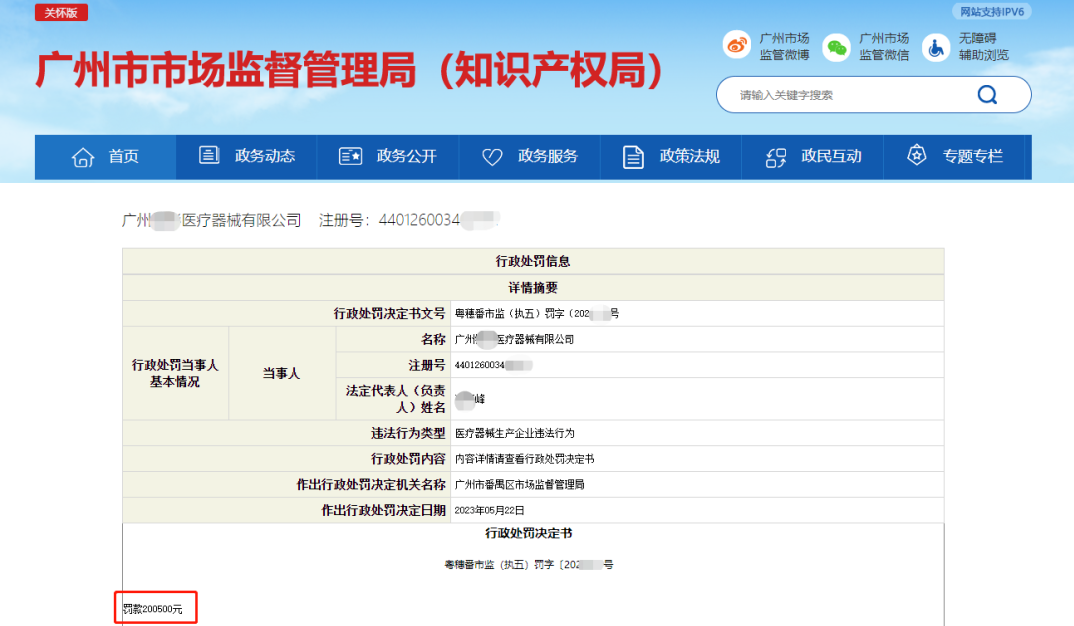
近日,廣州市市場監督管理局官網公布一則行政處罰信息,廣州一醫械企業因生產違反質量管理體系有關要求的產品,被罰205000元。
《醫療器械監督管理條例》第三十五條指出:醫療器械注冊人、備案人、受托生產企業應當按照醫療器械生產質量管理規范,建立健全與所生產醫療器械相適應的質量管理體系并保證其有效運行。
第三十六條則指出:醫療器械的生產條件發生變化,不再符合醫療器械質量管理體系要求的,醫療器械注冊人、備案人、受托生產企業應當立即采取整改措施;可能影響醫療器械安全、有效的,應當立即停止生產活動,并向原生產許可或者生產備案部門報告。
《醫療器械監督管理條例》第八十一條:有下列情形之一的,由負責藥品監督管理的部門責令改正,沒收違法生產經營使用的醫療器械;違法生產經營使用的醫療器械貨值金額不足1萬元的,并處2萬元以上5萬元以下罰款;貨值金額1萬元以上的,并處貨值金額5倍以上20倍以下罰款;情節嚴重的,責令停產停業,直至由原發證部門吊銷醫療器械注冊證、醫療器械生產許可證、醫療器械經營許可證,對違法單位的法定代表人、主要負責人、直接負責的主管人員和其他責任人員,沒收違法行為發生期間自本單位所獲收入,并處所獲收入30%以上3倍以下罰款,10年內禁止其從事醫療器械生產經營活動:
(一)生產、經營、使用不符合強制性標準或者不符合經注冊或者備案的產品技術要求的醫療器械;
(二)未按照經注冊或者備案的產品技術要求組織生產,或者未依照本條例規定建立質量管理體系并保持有效運行,影響產品安全、有效;
(三)經營、使用無合格證明文件、過期、失效、淘汰的醫療器械,或者使用未依法注冊的醫療器械;
(四)在負責藥品監督管理的部門責令召回后仍拒不召回,或者在負責藥品監督管理的部門責令停止或者暫停生產、進口、經營后,仍拒不停止生產、進口、經營醫療器械;
(五)委托不具備本條例規定條件的企業生產醫療器械,或者未對受托生產企業的生產行為進行管理;
(六)進口過期、失效、淘汰等已使用過的醫療器械。
經常關注我們的朋友一定發現了,我們分享過不少醫療器械企業違法生產/經營的案例(“違法案例”合集里已有20多條內容),但我們的初衷并非“落井下石”,只是想讓更多企業意識到合規的重要性。事實上,各監督部門對企業的處罰也只是手段而非目的,真正目的是給更多企業帶來一定的警示作用。
不論是生產企業還是經營企業,都需按規定辦理好相應證件,這并非為了應對國家監管,而是為了企業自身的長遠利益考慮,假如企業因為眼前一點利益而鋌而走險,其后定將后患無窮。金飛鷹,國內外醫療器械注冊一站式服務平臺,為醫械企業的合規經營(生產)保駕護航!
醫療器械注冊咨詢認準金飛鷹
深圳:0755-86194173
廣州:020 - 82177679
湖南:0731-22881823
四川:028 - 68214295